2018年Q3纳入药品优先审评品种分析
文丨赵成龙
2018年7月至9月,我国共有83个受理号的药品被纳入优先审评。
我国现行的药品优先审评制度是在推进药品审评审批改革、解决药品审评积压的背景下确立实施的,自2016年7月国家药审中心发布《“首仿”品种试行优先审评评定的基本原则》以来,我国已经共有18类药品被列入优先审评支持范围。
1、药品优先审评进展概况
药品优先审评制度实施以来,全国已经共有660个受理号的药品被纳入了优先审评,包括415个国产药品和245个进口药品,391个新药申请和269个仿制药申请。
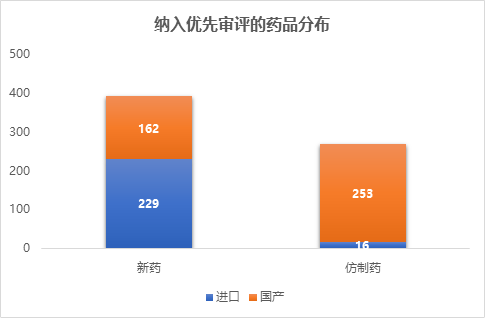
2018年第三季度,共有83个受理号的药品被纳入优先审评,较第二季度减少了17%。至此,2018年前三季度共有227个药品纳入优先审评,较去年同期增加了44.6%。从历年各季度纳入优先审评的药品数量上来看,除了开始实施的2016年情况特殊,2018年相比于上一年,纳入的药品数量有了大幅提升,仅前三季度的总数量就已经逼近了2017年全年的数量。
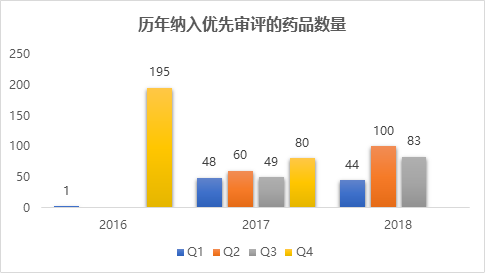
2018年Q3被纳入优先审评的药品中,新药申请32个,包含24个化药、7个生物制品和1个中药,仿制药51个,均为化药,因此化药总数为75个,占全部的90%;国产药品68个,进口药品申请15个,包含9个临床申请和6个生产申请。
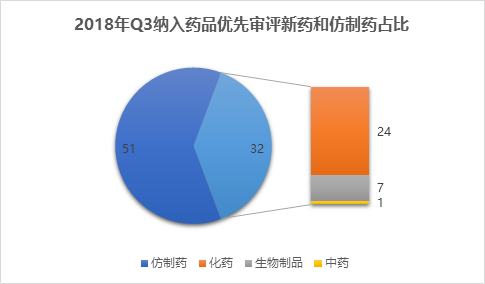
从入选理由来看,以“同一生产线生产并已有产品在美国、欧盟国家等上市”入选名单的品种最多,“罕见病”和“与现有治疗手段相比具有明显优势”位列二三。
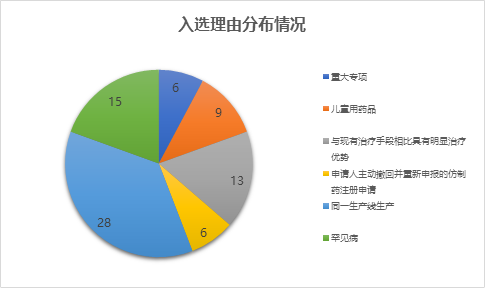
从注册申请人的地域分布情况来看,68个国产药品最主要分布在广东、江苏、浙江和山东,北京仅有4个,上海在三季度则并无药品被纳入优先审评。
从申请人和品种的分布情况来看,齐鲁制药及其海南公司共有10个药品被纳入优先审评,总数上排在第一,包括了2个规格的注射用培美曲塞二钠、4个规格的他达拉非片和4个规格的依托考昔片;紧随其后的是爱可泰隆医药贸易(上海)有限公司8个规格的进口药Selexipag片和1个波生坦分散片;排在后面的是东阳光药(6个)和海正药业(5个),以及均有4个药品被纳入的吉林津升制药和豪森药业。
2、重点药物简介
Selexipag片:爱可泰隆的Selexipag片是以国际多中心临床试验数据申请进口的罕见病药物,用于治疗目前致病因素尚不清楚、也尚无治愈手段的肺动脉高压(PAH)。Selexipag是爱可泰隆的第三款治疗PAH的药物,在其之前的马昔腾坦(Opsumit)和波生坦(Tracleer)均给爱可泰隆带来了长期的增长,波生坦片更是这家欧洲生物技术公司的支柱产品,占据了公司80%的销售额,。有瑞士信贷银行的分析师预测Selexipag这款药物到 2020 年的销售额可以达到 5.75 亿瑞士法郎(6.55 亿美元)。
KW-136胶囊:NS5A抑制剂KW-136胶囊是凯因科技具有自主知识产权的丙肝一类新药,作为重大专项被纳入药品优先审评,其与与索磷布韦片联合使用成为国内首个全口服、全基因型的丙肝根治方案。
马来酸艾维替尼:马来酸艾维替尼是由艾森医药自主研发的国内首个第三代EGFR抗肿瘤靶向抑制剂,也是原创国产1.1类新药,拥有全球化合物专利,用于治疗具有EGFR突变或耐药突变的非小细胞肺癌,作为十三五国家“重大新药创制”科技重大专项而被纳入药品优先审评。
重组人乳头瘤病毒16/18型双价疫苗(大肠杆菌):厦门万泰与厦门大学联合研制的重组人乳头瘤病16/18型双价疫苗是国内首支进入临床试验的国产重组人乳头瘤病毒疫苗,目前国产HPV疫苗的研发竞争非常激烈,有包括厦门万泰、成都生物制品研究所、上海泽润生物、上海博唯生物等在内的多家公司的6款产品处于临床试验阶段,而厦门万泰获得优先审评的二价HPV疫苗,无疑将成为有望最快上市的国产HPV疫苗。
格隆溴铵注射液:格隆溴铵注射液是一种抗胆碱能药物。目前国内仅有格隆溴铵片获批上市,尚未有该药品注射剂获批上市。2012年至今,国内有恒瑞医药、成都苑东和广东嘉博制药等8家企业获得格隆溴铵注射液临床批件,目前仅有恒瑞医药提交上市申请。2017年格隆溴铵注射液全球销售额约为1.89亿美元。
盐酸伐地那非片:盐酸伐地那非片是一种PDE5抑制剂,用于治疗男性勃起功能障碍,其原研由拜耳和GSK联合开发。科伦药业是国内首家盐酸伐地那非片通过生物等效性研究(BE)并以与原研质量一致性标准申报生产的企业。
*声明:本文由入驻新浪医药新闻作者撰写,观点仅代表作者本人,不代表新浪医药新闻立场。
- 聚力拓市启新程 吉享绿城焕生机
— 王老吉药业亮相广药南宁招商大会 以 “签约赋能 + 嗦粉...
- 国内首个治疗良性前列腺增生复方制剂“爱廷
3月22日下午,爱廷列“基层前列腺健康行”公益项目启动会暨上...
- 仑卡奈单抗和多奈单抗的巅峰对决!
目前医学界普遍认为,大脑中β淀粉样蛋白(Aβ)的异常沉积是阿...
- 仑卡奈单抗上市已一年,中国阿尔茨海默病治
在全球老龄化加速的背景下,阿尔茨海默病(Alzheimer’...


